兰州大学泛第三极环境中心以“Semi-rational design of psychrophilic cellobiose 2-epimerase for improved substrate affinity and enhanced low-temperature epimerization activity”为题,发表于《Bioresource Technology》期刊,该成果第一作者为2022级博士研究生徐虎,刘勇勤教授为通讯作者。本研究提出的整合半理性设计与荧光筛选的策略,成功改善了嗜冷酶活性与底物亲和力难以兼顾的天然缺陷。该研究不仅提供了一种高效的冷活性生物催化剂,也为嗜冷酶的工程化改造建立了一种通用的筛选平台。
冷活性酶在乳制品加工行业中具有重要应用前景。冷链加工不仅能最大限度地保留热敏性营养成分并改善产品风味,还能显著提升乳制品的整体营养价值。然而,要在低温条件下实现乳糖向依匹乳糖的高效生物转化,高度依赖具备优异低温活性的冷活性纤维二糖差向异构酶(CE)。来源自青藏高原冰川的嗜冷纤维二糖差向异构酶(psyCE)是首个被鉴定的嗜冷CE,也是目前已报道冷活性CE中催化常数(kcat)最高的酶。嗜冷酶通常具有较高的结构柔性以维持低温下的催化活性,但这种高柔性往往伴随着底物亲和力低(高Km)代价,即“活性-亲和力权衡”。因此,要开发满足工业需求的更加高效的低温催化剂,需要通过酶工程改造来改善底物亲和力与活性之间的权衡关系。另外,目前仍然缺乏稳定高效的针对CE的突变体筛选策略,不同克隆间蛋白表达水平的差异常导致筛选结果出现假阳性。针对上述瓶颈,本研究结合半理性设计,开发一种基于绿色荧光蛋白(GFP)的蛋白浓度归一化的辅助筛选系统,成功获得psyCE高性能突变体(FR)。本研究不仅通过系统的酶学性质表征证实了该突变体卓越的低温催化能力,还结合分子动力学模拟探讨了活性位点重塑提升酶催化效率的分子机制。
使用融合表达策略构建GFP辅助筛选系统,基于GFP荧光强度与可溶性蛋白表达量的正相关性对突变库进行半定量评价。该方法通过测定96孔板内各突变克隆粗酶液的GFP荧光信号,以最低有效信号为基准对其余孔位进行等比例稀释,实现各样本间酶浓度的归一化。该方法处理得到的每个反应体系内部具有相同的初始酶量,并能与HPLC产物检测结果直接关联,有效排除了因细胞生长或蛋白表达差异导致的假阳性,实现了对突变体真实催化活性的精准评估(图1)。
图2显示,所有突变体的最适温度(35°C)、最适pH(7.5)以及整体的热失活曲线均与野生型(WT)保持一致。在5个突变体中,FR展现出最快的反应速率和最高的产物生成率。酶促动力学分析表明,FR突变体的Km值从WT的261.9 mM显著降低至208.9 mM,同时其kcat提升至245.7 s−1,再次刷新了已知冷活性CE的kcat纪录。
结构分析表明,FR突变体底物结合口袋的体积和表面积实现了显著扩展(相比WT近乎翻倍)。同时,在FR-乳糖复合物中,底物乳糖的溶剂可及表面积(SASA)显著降低,而复合物的包埋表面积(BSA)相应增大。这些结果表明,该突变策略促进了蛋白与底物更加紧密的结合(图3)。
分子动力学模拟进一步揭示,FR突变体不仅增加了蛋白-底物之间氢键的数量,还大幅提升了氢键网络的持久性(连续氢键寿命显著延长)。同时,其底物-溶剂氢键数量显著减少。这些动态特征表明,该突变体成功重塑并强化了稳定底物结合的氢键相互作用网络(图4)。
在结合能层面,FR突变体展现出更低的总结合自由能(ΔG),并在关键的静电作用和范德华力等能量项上获得显著增强。残基能量分解分析进一步表明,FR突变体中参与稳定底物的关键氨基酸数量明显增多,形成了更为广泛的作用网络,从而从热力学角度印证了其在底物亲和力方面的显著优势(图5)。
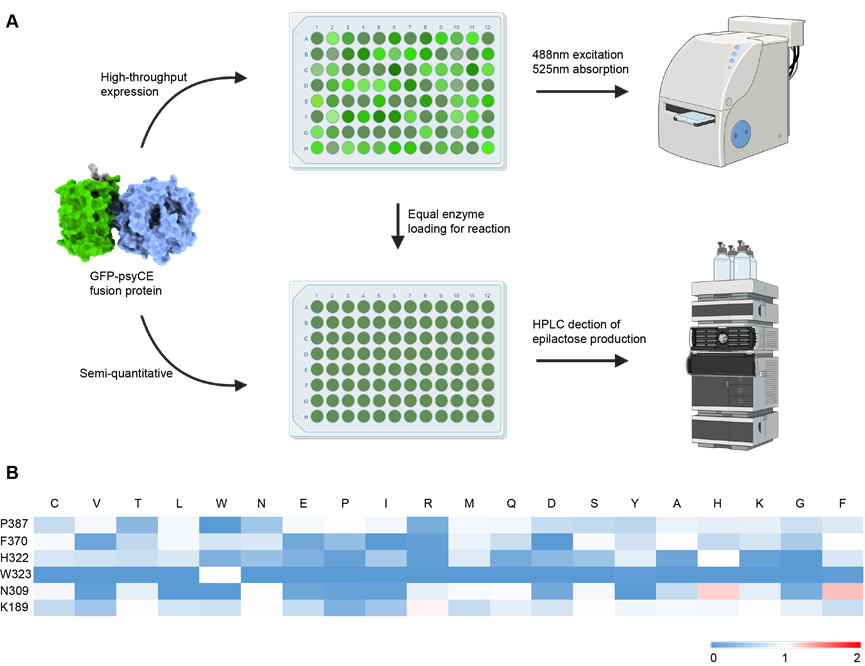
图1:荧光辅助筛选过程及结果。(A)基于GFP-psyCE作为模板的荧光辅助突变体筛选示意图。(B)荧光辅助突变体筛选结果,红色表示活性提高。
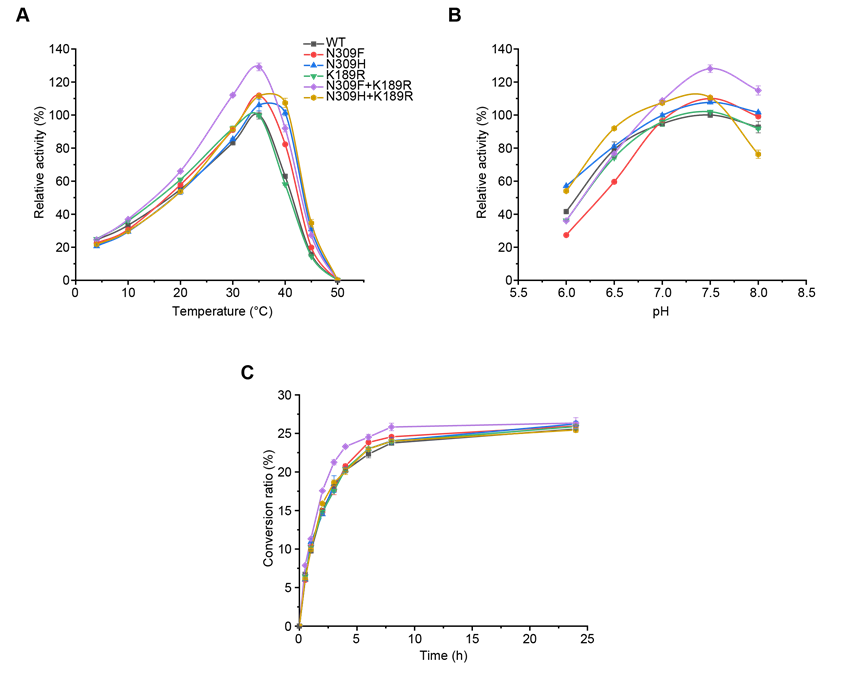
图2:psyCE野生型(WT)及其突变体的催化性能比较。psyCE及其突变体的温度(A)和pH(B)曲线。(C)依匹乳糖生成的时间进程研究。

图3:底物结合口袋与溶剂可及表面积分析。可视化WT(A)和FR(B)的底物结合口袋。WT和FR的apo蛋白(C)、复合物中的蛋白(D)、复合物中的底物(E)和整个复合物(F)的SASA比较。
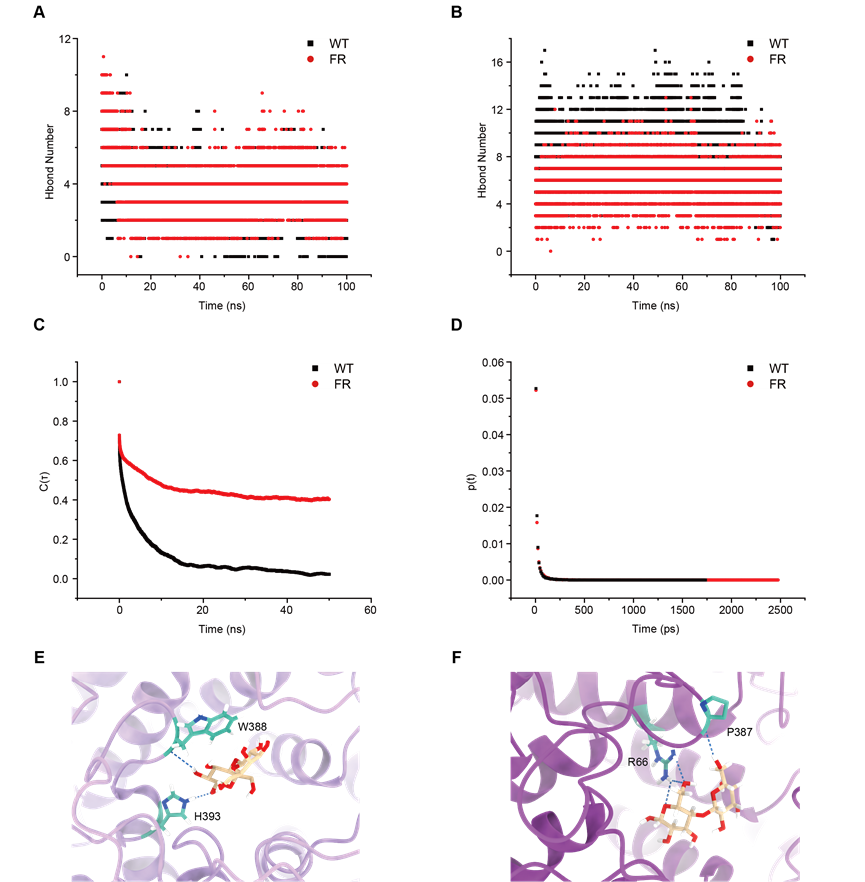
图4:底物相互作用的氢键分析。(A)底物与酶之间的氢键数量比较。(B)底物与溶剂之间的氢键数量比较。(C)底物-酶相互作用的氢键自相关函数比较。(D)底物与酶之间连续氢键寿命分布比较。从WT(E)和FR(F)分子动力学模拟中自由能景观全局最小值对应的代表性构象中提取氢键网络。

图5:MM/GBSA结合自由能分析。(A)WT和FR系统中乳糖的总结合自由能。(B)WT和FR系统中结合自由能组分的分解。WT系统(C)和FR系统(D)中距离乳糖4 Å以内的残基的结合自由能逐个残基分解。EVDWAALS为范德华力;EEL为静电能;EGB为极性溶剂化自由能;ESURF为非极性溶剂化自由能;GGAS(气相能量)= EVDWAALS + EEL;GSOLV(总溶剂化自由能)= EGB + ESUFR;ΔG(总自由能)= GGAS + GSOLV。



